Encyklopedie fyziky |
| NASTAVENÍ TISKU (tato tabulka nebude vytištěna) | Zpět k článku | Vytiskni! | |
| Komentáře [1x] - Skrýt | Nadstandardní komentář [0x] | Definice [2x] - Skrýt |
Lithiové akumulátory
První lithiové články byly vynalezeny již v 60. letech 20. století. Od počátku se vyznačovaly těmito vlastnostmi:
1. relativně velká kapacita akumulátoru;
2. relativně pomalé samovybíjení;
3. byly snadno vyrobitelné ve variantě, kterou bylo možno dobíjet.
Přesto první články nebyly dlouhodobě použitelné. Příčinou byl fakt, že kladná elektroda byla vyrobená ze sulfidů kovů a záporná elektroda byla vyrobena z lithia, čímž nastávala relativně rychle a snadno koroze a pasivace obou elektrod.
Pasivace elektrod je chemický jev, při kterém se tvoří kompaktní vrstva sloučenin na elektrodách vlivem styku kovových elektrod a elektrolytu. Takto vytvořená vrstva pak brání přístupu iontů elektrolytu na elektrody.
Zlom ve vývoji článků nastal v roce 1990, kdy byla uvedena na trh technologie využívající různé příměsi pro výrobu elektrod. Právě proto se začal používat název Li-ion, který je složeninou chemické značky lithia a zkratkou ze slova iont.
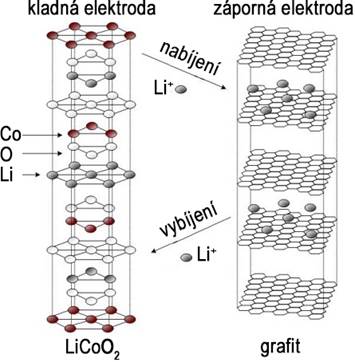
Lithiové akumulátory jsou akumulátory s bezvodým elektrolytem - nejčastěji lithium hexaflorofosfát ![]() v nepolárním organickém rozpouštědle. Jako kladná elektroda se používá oxid lithia a dalšího kovu (kobalt, mangan, nikl, …). Záporná elektroda je vyrobena z uhlíkového materiálu (většinou grafit). Během nabíjení akumulátoru se ionty lithia přesouvají z kladné elektrody na zápornou. Atomy lithia se přitom velmi snadno ionizují na jednomocné ionty.
v nepolárním organickém rozpouštědle. Jako kladná elektroda se používá oxid lithia a dalšího kovu (kobalt, mangan, nikl, …). Záporná elektroda je vyrobena z uhlíkového materiálu (většinou grafit). Během nabíjení akumulátoru se ionty lithia přesouvají z kladné elektrody na zápornou. Atomy lithia se přitom velmi snadno ionizují na jednomocné ionty.
Zásadním rozdílem oproti jiným typům akumulátorů je, že ionty lithia pouze tzv. interkalují do struktury záporné elektrody. Proto na záporné elektrodě neprobíhá chemická reakce, což vede k dlouhé životnosti akumulátoru bez velkých změn ve výkonu akumulátoru.
Interkalovat znamená vmístit se do krystalové mřížky materiálu bez chemické reakce se samotným materiálem.
Je-li kladná elektroda tvořena lithium-kobalt oxidem ![]() (viz obr. 110), probíhá na kladné elektrodě při nabíjení oxidace kobaltu: iont
(viz obr. 110), probíhá na kladné elektrodě při nabíjení oxidace kobaltu: iont ![]() přechází na iont
přechází na iont ![]() . Při vybíjení pak nastává redukce kobaltu: iont
. Při vybíjení pak nastává redukce kobaltu: iont ![]() přechází na iont
přechází na iont ![]() . Souhrnně lze psát:
. Souhrnně lze psát: ![]() . Na záporné elektrodě pak probíhá vratná reakce
. Na záporné elektrodě pak probíhá vratná reakce ![]() .
.
Elektromotorické napětí akumulátoru je ve srovnání s ostatními typy vyšší: u lithiových akumulátorů dosahuje až 3,7 V na jeden článek. Energetická hustota je vyšší než u ostatních typů akumulátorů z velké části právě kvůli vyššímu napětí. Vybíjecí napěťová křivka je relativně plochá, což znamená, že napájené zařízení má po dlouhou dobu téměř konstantní vstupní napětí. V té souvislosti je ale také obtížnější zjistit přesný stav nabití akumulátoru.
 |
| Obr. 110 |
Mezi hlavní výhody lithiových akumulátorů patří:
1. nezávadnost pro životní prostředí - akumulátory neobsahují rtuť, olovo, kadmium, …;
2. relativně dlouhá životnost - akumulátor vydrží 500 až 1500 nabíjecích a vybíjecích cyklů;
3. nemají paměťový efekt;
Před nabíjením tedy nemusí být akumulátor zcela vybit.
4. relativně nízké samovybíjení (přibližně 8 % kapacity baterie za měsíc);
5. relativně velká energie uložená v akumulátoru - od 2000 mWh po 7200 mWh;
6. relativně malá hmotnost akumulátoru.
Mezi nevýhody těchto akumulátorů patří:
1. lithium a jeho sloučeniny na vzduchu (a zejména při styku s vlhkostí) reagují a degradují, proto se musí s akumulátory manipulovat velmi opatrně;
2. relativně velký vnitřní odpor;
3. výkon akumulátoru s klesající teplotou klesá;
4. pokles napětí při vybíjení, což může být nepříjemné pro zařízení, která potřebují konstantní napětí;
5. vyžadují pouze jeden konkrétní typ nabíječe (nelze používat jeden nabíječ pro různé typy lithiových akumulátorů);
6. zpočátku se prodávaly za relativně vysokou cenu.