Encyklopedie fyziky |
| NASTAVENÍ TISKU (tato tabulka nebude vytištěna) | Zpět k článku | Vytiskni! | |
| Komentáře [1x] - Skrýt | Nadstandardní komentář [0x] | Definice [0x] |
Vzájemné působení částic. Potenciální energie částic
Tuto složitou situaci si zjednodušíme - zaměříme se jen na dvě částice, jejichž kladně nabitá jádra jsou obklopena záporně nabitými elektrony. Při vzájemném přibližování těchto částic interagují mezi sebou elektronové obaly a kladně nabitá jádra. Při malých vzdálenostech je tato síla odpudivá, při větších přitažlivá.
To je známo z praxe: při stlačování tělesa pociťujeme odporovou sílu, která brání dalšímu stlačování tělesa, zatímco při snaze těleso prodloužit vnímáme sílu bránící dalšímu prodlužování.
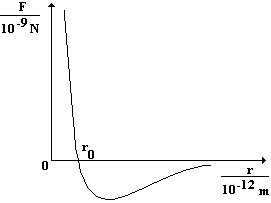
Na obr. 1 je znázorněna grafická závislost velikosti síly F, která působí mezi dvěma částicemi, na jejich vzájemné vzdálenosti r. Velikost přitažlivé síly se nanáší pod osu r, velikost odpudivé síly nad tuto osu.
Z grafu je možné vyčíst následující vlastnosti interakce dvou částic:
1. Při určité vzdálenosti ![]() (řádově setiny až desetiny nm) je velikost síly, kterou na sebe částice vzájemně působí, nulová. Obě částice jsou v rovnovážné poloze.
(řádově setiny až desetiny nm) je velikost síly, kterou na sebe částice vzájemně působí, nulová. Obě částice jsou v rovnovážné poloze.
2. Ve vzdálenosti větší než ![]() je tato síla přitažlivá - její velikost se nejdříve zvětšuje a potom s rostoucí vzdáleností se její účinek rychle zmenšuje. Při velké vzdálenosti je tato síla zanedbatelně malá, z čehož plyne, že každá částice je přitahována jen nejbližšími částicemi ve svém okolí. (U kapalin se přitažlivé působení projevuje do vzdálenosti asi 1 nm.)
je tato síla přitažlivá - její velikost se nejdříve zvětšuje a potom s rostoucí vzdáleností se její účinek rychle zmenšuje. Při velké vzdálenosti je tato síla zanedbatelně malá, z čehož plyne, že každá částice je přitahována jen nejbližšími částicemi ve svém okolí. (U kapalin se přitažlivé působení projevuje do vzdálenosti asi 1 nm.)
3. Ve vzdálenosti menší než ![]() působí mezi částicemi síla odpudivá, jejíž velikost rychle roste se zmenšující se vzdáleností.
působí mezi částicemi síla odpudivá, jejíž velikost rychle roste se zmenšující se vzdáleností.
 |
| Obr. 1 |
Síly, jimiž na sebe působí částice atomy v molekule, se nazývají vazebné síly - při slučování atomů vzniká chemická vazba mezi atomy. Vazebné síly určují strukturu molekul (vzájemnou polohu částic), která je důležitá nejen pro chemii, fyziku a biologii, ale i pro další (aplikované) obory - medicínu, zemědělství, …:
1. dvouatomové molekuly - lineární
2. tříatomové molekuly - lineární (např. ![]() ), ale většinou jako rovinné - trojúhelníkové (
), ale většinou jako rovinné - trojúhelníkové (![]() )
)
3. víceatomové molekuly - nejčastěji prostorové (![]() má tvar trojbokého jehlanu) nebo rovinné (benzen
má tvar trojbokého jehlanu) nebo rovinné (benzen ![]() )
)
Z existence vzájemného působení částic také vyplývá, že daná soustava částic má potenciální energii. Pro rovnovážnou polohu částic se tato energie nazývá vazebná energie. Ta je rovna práci, kterou bychom museli vykonat působením vnějších sil, abychom zrušili vazby mezi jednotlivými částicemi.