Encyklopedie fyziky |
| NASTAVENÍ TISKU (tato tabulka nebude vytištěna) | Zpět k článku | Vytiskni! | |
| Komentáře [1x] - Zobrazit | Nadstandardní komentář [0x] | Definice [0x] |
Vazba sigma a vazba pí
Vznik vazby ![]() je podmíněn obsazením vazebného molekulového orbitalu
je podmíněn obsazením vazebného molekulového orbitalu ![]() . Tento orbital je charakterizován velkou elektronovou hustotou na spojnici dvou atomových jader atomů účastnících se dané vazby. Tato vazba je nepohyblivá a vzniká při přechodu elektronů z atomových orbitalů do molekulového orbitalu, čímž se sníží energie systému. Molekulový orbital, do kterého přejdou elektrony, se nazývá vazebný molekulový orbital.
. Tento orbital je charakterizován velkou elektronovou hustotou na spojnici dvou atomových jader atomů účastnících se dané vazby. Tato vazba je nepohyblivá a vzniká při přechodu elektronů z atomových orbitalů do molekulového orbitalu, čímž se sníží energie systému. Molekulový orbital, do kterého přejdou elektrony, se nazývá vazebný molekulový orbital.
V chemické vazbě se vždy vyskytuje vazba ![]() . Násobné vazby jsou tvořeny jednou vazbou
. Násobné vazby jsou tvořeny jednou vazbou ![]() a ostatní vazby jsou vazby
a ostatní vazby jsou vazby ![]() .
.
Orbital ![]() může vzniknout kombinací (resp. překryvem):
může vzniknout kombinací (resp. překryvem):
1. dvou orbitalů s;
2. dvou orbitalů p;
3. orbitalu p a orbitalu s.
Schematicky je tento překryv orbitalů zobrazen na obr. 71.
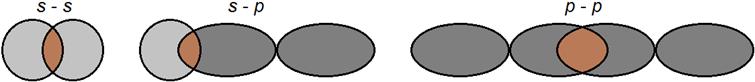 |
| Obr. 71 |
Vazba ![]() vzniká překryvem dvou orbitalů p tak, že největší elektronová hustota není na spojnici jader obou atomů účastnících se vazby, ale nad nebo pod touto spojnicí (viz schematicky obr. 72). Přímo na spojnici obou jader je elektronová hustota nulová. Překryvem dvou orbitalů p vzniká vazebný molekulový orbital
vzniká překryvem dvou orbitalů p tak, že největší elektronová hustota není na spojnici jader obou atomů účastnících se vazby, ale nad nebo pod touto spojnicí (viz schematicky obr. 72). Přímo na spojnici obou jader je elektronová hustota nulová. Překryvem dvou orbitalů p vzniká vazebný molekulový orbital ![]() , který je příčinou vzniku pohyblivé vazby
, který je příčinou vzniku pohyblivé vazby ![]() (delokalizované vazby
(delokalizované vazby ![]() ).
).
Delokalizovaný objekt je takový, který nelze s jistotou lokalizovat. Lokalizované je auto s krabičkou GPS - jeho poloha je v každém okamžiku na celé jeho trajektorii známá. Delokalizovaný je pes, který na jaře vyběhne ze zahrady a běhá v okolí za každou fenkou. Nemá-li takový pes žádné čipování a podobně, je delokalizovaný - jeho poloha není přesně známa. Ví se jen, že pobíhá někde po okolí, ale u které fenky právě je, není možné říci.
U vazby ![]() mohou vzniknout dva orbitaly
mohou vzniknout dva orbitaly ![]() se stejnou energií (takovým orbitalům se pak říká degenerované orbitaly).
se stejnou energií (takovým orbitalům se pak říká degenerované orbitaly).
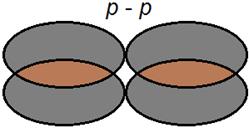 |
| Obr. 72 |