Encyklopedie fyziky |
| NASTAVENÍ TISKU (tato tabulka nebude vytištěna) | Zpět k článku | Vytiskni! | |
| Komentáře [7x] - Zobrazit | Nadstandardní komentář [1x] - Zobrazit | Definice [0x] |
Interakce kovu a roztoku
V krystalu kovu je každý vnitřní atom obklopen většinou osmi nebo dvanácti stejnými atomy, s nimiž je bezprostředně vázán.
Tento fakt vyplývá z uspořádání jednotlivých atomů do krystalové mříže. V závislosti na typu mříže má daný atom různý počet sousedních atomů.
Atomy kovů ale mají menší počet valenčních elektronů, než který by byl potřeba k vytvoření např. kovalentní vazby. Proto žádný z valenčních elektronů nepřísluší v krystalu kovu dvěma konkrétním atomům, ale všem atomům v krystalu současně. Tento jev popisujeme tak, že v kovové vazbě jsou elektrony delokalizovány a vytvářejí tak elektronový plyn.
Zjednodušeně si můžeme představit, že krystal kovu je tvořen kationty, které jsou umístěny v uzlových bodech krystalové mřížky a v prostoru mezi nimi se volně pohybují elektrony (to jsou ty delokalizované elektrony).
Z tohoto hlediska se tedy struktura kovů podobá struktuře iontových sloučenin.
Pro vyšetřování elektrolýzy ve vodním roztoku lze tedy předpokládat následující děje, které lze sledovat na schematickém obr. 99:
1. při styku kovového krystalu s vodou nastává zhruba podobný děj, jako nastává v případě rozpouštění iontového krystalu ve vodě;
2. účinkem polárních molekul vody se určité množství kationtů kovů odštěpuje z krystalové struktury a přechází do vody (viz obr. 99b));
3. elektrony ze struktury kovů se nemůžou odštěpit a zůstávají uvnitř kovu.
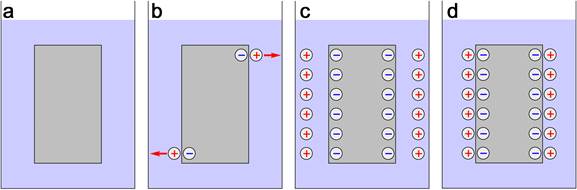 |
| Obr. 99 |
1. kovová elektroda se nabíjí záporně a roztok kladně (viz obr. 99c));
Pokud se z kovu oddělují jeho kationty, tak ty odnášejí kladný náboj. Ve zbytku kovu tedy převažují elektrony, proto se kov nabíjí záporně. Kationty kovu jsou odnášeny do roztoku, který se proto nabíjí kladně.
2. záporně nabitá elektroda začíná přitahovat kationty, které přešly do roztoku;
Mezi záporně nabitou elektrodou a kationtem kovu (kladně nabitý iont) působí přitažlivá elektrostatická síla.
3. pokud počet uvolněných kationtů do roztoku je za jednotku času stejný, jako počet kationtů vázaných vlivem elektrostatické síly k elektrodě, nastává rovnovážný stav;
4. na povrchu elektrody se tak vytváří tzv. elektrická dvojvrstva, která je tvořena kladně a záporně nabitými částicemi (viz obr. 99d)).
Takto vytvořená elektrická dvojvrstva pak brání přechodu dalších iontů do roztoku a z roztoku na elektrodu. To znamená, že tato dvojvrstva brání průchodu elektrického proudu roztokem.
Popsaná situace nastává např. v případě ponoření zinkové elektrody do vody.
Ponoříme-li kovovou elektrodu do roztoku soli daného kovu, budou probíhat odlišné děje, než byly popsány v předchozím případě. Tyto děje, které jsou schematicky zobrazeny na obr. 100, jsou:
1. rozštěpení molekul soli kovů na kationt kovu a záporný aniont (viz obr. 100b));
2. kationty kovu elektrody začínají přecházet do roztoku, ale v menší míře, než by přecházely do vody (viz obr. 100c));
Kationty kovu uvolněné z elektrody do roztoku jsou stejné jako kationty vzniklé v roztoku rozštěpením jeho molekul.
3. je-li koncentrace kationtů v roztoku dostatečně velká, klesne schopnost kovu uvolňovat další kationty do roztoku, a proto se část kationů kovu vyloučí z roztoku přímo na povrch kovu;
4. kov se uvedeným mechanismem nabije kladně a v důsledku toho se roztok nabije záporně (viz obr. 100d));
5. mezi roztokem a povrchem kovu vzniká určitý potenciálový rozdíl, který se nazývá standardní elektrodový potenciál ![]() daného kovu (viz obr. 101).
daného kovu (viz obr. 101).
Symbol ![]() označuje fyzikální veličinu, ale neznamená veličinu umocněnou na nultou! „0“ v horním indexu je symbol, nikoliv číslo nula!
označuje fyzikální veličinu, ale neznamená veličinu umocněnou na nultou! „0“ v horním indexu je symbol, nikoliv číslo nula!
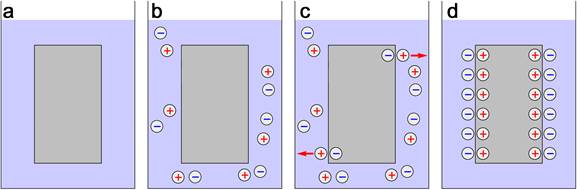 |
| Obr. 100 |
Elektrodový potenciál bychom tedy mohli měřit. Situace zobrazená na obr. 101 je ovšem pouze schematická - takto standardní elektrodový potenciál daného kovu měřit nelze (viz dále).
Vzhledem k tomu, že se jedná o potenciál mezi dvěma místy (kovová elektroda a roztok), měli bychom mluvit správně o elektrickém napětí mezi elektrodou a roztokem. Důvod, proč se mluví o potenciálu, vyplývá z faktu, že elektrický potenciál roztoku je velmi špatně neměřitelný. Proto je nutné měřit elektrický potenciál dané elektrody vůči jinému vztažnému potenciálu (referenčnímu potenciálu) standardní elektrody. A proto je pak i jednodušší dále uvažovat elektrodový potenciál (daného kovu) než elektrodové napětí.
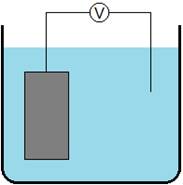 |
| Obr. 101 |
Popsaná situace nastává při ponoření měděné elektrody do roztoku síranu měďnatého, zinkové elektrody do roztoku síranu zinečnatého, …, ale i při ponoření např. měděné elektrody do vody. To, která ze dvou výše popsaných variant (zobrazených na obr. 99 a obr. 100) nastane, vyplývá z hodnoty elektrodového potenciálu daného kovu. Na základě tohoto potenciálu jsou kovy seřazeny do tzv. Beketovovy řady kovů.
Ponořením obou typů výše popsaných elektrod do roztoku s volnými nosiči náboji (ionty a elektrony) vzniká mezi oběma elektrodami elektrické napětí. To způsobí, že roztokem může procházet elektrický proud.
Popsané napětí je v tomto případě dáno rozdílem standardních elektrodových potenciálů obou kovů, z nichž jsou elektrody vyrobeny.