Encyklopedie fyziky |
| NASTAVENÍ TISKU (tato tabulka nebude vytištěna) | Zpět k článku | Vytiskni! | |
| Komentáře [0x] | Nadstandardní komentář [3x] - Zobrazit | Definice [1x] - Zobrazit |
Střední kvadratická rychlost
Okamžitá rychlost molekuly pohybující se neuspořádaným posuvným pohybem je náhodná a stále se měnící veličina, která nám nic o chování plynu neřekne. Proto se používají statistické veličiny. Předpokládejme, že plyn uzavřený v nádobě obsahuje N molekul stejné hmotnosti ![]() . Z tohoto počtu má v důsledku neuspořádaného pohybu
. Z tohoto počtu má v důsledku neuspořádaného pohybu ![]() molekul velikost rychlosti v intervalu
molekul velikost rychlosti v intervalu ![]() . Celková kinetická energie molekul konajících neuspořádaný posuvný pohyb je:
. Celková kinetická energie molekul konajících neuspořádaný posuvný pohyb je: ![]() .
.
Nyní je možné si představit, že se všechny molekuly daného plynu pohybují stejně velkou rychlostí ![]() , kterou volíme tak, aby celková kinetická energie
, kterou volíme tak, aby celková kinetická energie ![]() zůstala nezměněná. Rychlost
zůstala nezměněná. Rychlost ![]() se pak nazývá střední kvadratická rychlost a je to statistická veličina. Z právě uvedené definice vyplývá:
se pak nazývá střední kvadratická rychlost a je to statistická veličina. Z právě uvedené definice vyplývá: ![]() , odkud dostáváme
, odkud dostáváme ![]() , kde
, kde ![]() . Druhá mocnina střední kvadratické rychlosti je tedy rovna součtu druhých mocnin rychlostí všech molekul dělených celkovým počtem molekul. (A je tudíž rovna aritmetickému průměru druhých mocnin rychlostí všech molekul.)
. Druhá mocnina střední kvadratické rychlosti je tedy rovna součtu druhých mocnin rychlostí všech molekul dělených celkovým počtem molekul. (A je tudíž rovna aritmetickému průměru druhých mocnin rychlostí všech molekul.)
Střední kvadratická rychlost molekul je taková rychlost, kterou se pohybují všechny molekuly daného ideálního plynu. Její hodnota je určena tak, že celková kinetická energie molekul plynu vypočtená pomocí této rychlosti je stejná jako součet kinetických energií všech molekul, které se pohybují obecně různými rychlostmi.
Kromě střední kvadratické rychlosti lze soubor molekul daného plynu charakterizovat dalšími význačnými velikostmi rychlostí: nejpravděpodobnější rychlostí ![]() a střední (průměrnou) rychlostí
a střední (průměrnou) rychlostí ![]() .
.
Nejpravděpodobnější rychlost je velikost rychlosti, pro níž nabývá rozdělovací funkce ![]() svého maxima. Velikost této rychlosti je dána vztahem
svého maxima. Velikost této rychlosti je dána vztahem ![]() . Střední rychlost (průměrná rychlost) je průměrem všech velikostí rychlostí, kterými se molekuly daného plynu pohybují. Její velikost je rovna
. Střední rychlost (průměrná rychlost) je průměrem všech velikostí rychlostí, kterými se molekuly daného plynu pohybují. Její velikost je rovna ![]() .
.
Pro základní představu a srovnání velikostí těchto rychlostí jsou všechny uvedené rychlosti vyznačeny na obr. 21. Konkrétně pro kyslík při teplotě 300 K dostáváme tyto hodnoty: ![]() ,
, ![]() a
a ![]() .
.
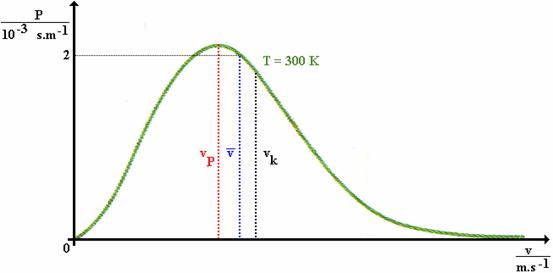 |
| Obr. 21 |