Encyklopedie fyziky |
| NASTAVENÍ TISKU (tato tabulka nebude vytištěna) | Zpět k článku | Vytiskni! | |
| Komentáře [0x] | Nadstandardní komentář [0x] | Definice [0x] |
Izotermický děj
je děj, při němž zůstává teplota plynu stálá - plyn o dané hmotnosti mění pouze svůj tlak a objem. Vzhledem k tomu, že platí ![]() , dostáváme stavovou rovnici ve tvaru
, dostáváme stavovou rovnici ve tvaru ![]() resp.
resp. ![]() : Při izotermickém ději s ideálním plynem stálé hmotnosti je součin tlaku a objemu plynu stálý (Boylův - Mariottův zákon).
: Při izotermickém ději s ideálním plynem stálé hmotnosti je součin tlaku a objemu plynu stálý (Boylův - Mariottův zákon).
Graf vyjadřující závislost tlaku plynu stálé hmotnosti jako funkci objemu při izotermickém ději se nazývá izoterma (viz obr. 22). Jedná o větev hyperboly, jejíž tvar je dán teplotou, při níž děj probíhá.
Vzhledem k tomu, že teplota je stálá, je stálá také střední kinetická energie molekul konajících neuspořádaný tepelný pohyb. Z toho tedy vyplývá, že vnitřní energie ideálního plynu je konstantní, tj. ![]() . První termodynamický zákon je tedy možné psát ve tvaru
. První termodynamický zákon je tedy možné psát ve tvaru ![]() : Teplo přijaté ideálním plynem při izotermickém ději se rovná práci, kterou plyn při tomto ději vykoná.
: Teplo přijaté ideálním plynem při izotermickém ději se rovná práci, kterou plyn při tomto ději vykoná.
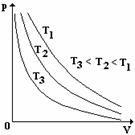 |
| Obr. 22 |