Encyklopedie fyziky |
| NASTAVENÍ TISKU (tato tabulka nebude vytištěna) | Zpět k článku | Vytiskni! | |
| Komentáře [2x] - Zobrazit | Nadstandardní komentář [0x] | Definice [0x] |
Atom vodíku
Podle Schrödingerova kvantově mechanického modelu se atomy mohou nacházet pouze v určitých stacionárních stavech s danou energií. Těmto stavům odpovídá určité, časově neproměnné rozložení hustoty pravděpodobnosti výskytu elektronů v elektronovém obalu. Najdeme je řešením Schrödingerovy rovnice pro pohyb elektronů v přitažlivém coulombovském silovém poli atomového jádra. Dostaneme tak vlnovou funkci ![]() a hustotu pravděpodobnosti výskytu elektronů udává čtverec její absolutní hodnoty
a hustotu pravděpodobnosti výskytu elektronů udává čtverec její absolutní hodnoty ![]() .
.
V tomto případě je ovšem situace mnohem složitější, než při pohybu jednoho elektronu vázaného na úsečku ve směru osy x.
Při pohybu elektronu po úsečce jsme uvažovali nejjednodušší možný případ: volný elektron (tj. elektron, na který nepůsobila žádná vnější síla). V případě pohybu elektronu kolem atomového jádra není toto přiblížení možné - na elektron totiž působí coulombovská přitažlivá síla!
Omezíme se na nejjednodušší atom - atom vodíku, který je tvořen jedním protonem a jedním elektronem. Atomy s větším počtem elektronů lze vyřešit jen pomocí přibližných matematických metod. Dále je dobré si uvědomit, že elektron se nyní pohybuje v okolí jádra v trojrozměrném prostoru a bude tedy vytvářet složité stojaté elektronové vlny.
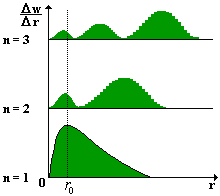
Je možné vyšetřovat např. jaká je pravděpodobnost výskytu elektronu v určité vzdálenosti r od jádra. Výsledek pro první tři hladiny je na obr. 42. Po srovnání s obr. 41 (rozložení pravděpodobností výskytu při pohybu volného elektronu) je vidět, že i v tomto případě existují vzdálenosti, v nichž se bude elektron vyskytovat s větší resp. nulovou pravděpodobností. V základním stavu najdeme elektron nejspíše ve vzdálenosti ![]() .
.
 |  |
| Obr. 42 | Obr. 43 |
Tato vzdálenost se nazývá Bohrův poloměr. Jak je vidět z obr. 42, křivka se pro větší vzdálenosti elektronu od jádra blíží k ose r asymptoticky, tj. existuje pravděpodobnost nalezení elektronu v libovolné vzdálenosti od jádra (i když je tato pravděpodobnost velmi malá).
S nadsázkou lze tedy říci, že každý atom vlastně zaujímá prostor celého vesmíru.
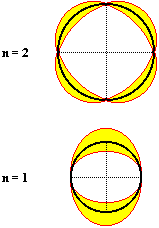
V různých kvantových stavech bude pravděpodobnost výskytu elektronu záviset také na směru. Elektronová vlna by nyní měla vytvořit stojaté vlnění na kulovém povrchu. Na obvodu hlavní kružnice uvažované koule se tedy rozloží celistvý násobek vlnových délek (viz obr. 43). Tím se ale rozložení pravděpodobnosti výskytu elektronu v prostoru dále komplikuje.
::subtree::