Vazba iontová
Tato vazba vzniká mezi atomem, který má malý počet elektronů ve valenční slupce a jejich ztrátou se přemění na kladně nabitý iont se zcela zaplněnou poslední vnější slupkou, a atomem, kterému se nedostává tento malý počet elektronů ve valenční slupce a jejich doplněním přejde v iont nabitý záporně.
Tuto vazbu lze najít např. u molekuly NaCl (schematicky znázorněno na obr. 67). Sodík ztrátou jediného elektronu z podslupky 3s vytvoří iont 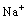 s elektronovou konfigurací neonu, chlor doplněním jednoho elektronu do podslupky 3p vytvoří iont
s elektronovou konfigurací neonu, chlor doplněním jednoho elektronu do podslupky 3p vytvoří iont 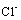 s elektronovou konfigurací argonu. Oba ionty se pak chemicky váží přitažlivými elektrostatickými silami v molekulu NaCl. Iontově vázaná molekula může ve vodném roztoku opět disociovat, tj. rozložit se na kladný a záporný iont a vytvořit elektrolyt.
s elektronovou konfigurací argonu. Oba ionty se pak chemicky váží přitažlivými elektrostatickými silami v molekulu NaCl. Iontově vázaná molekula může ve vodném roztoku opět disociovat, tj. rozložit se na kladný a záporný iont a vytvořit elektrolyt.
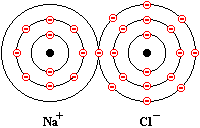 |
| Obr. 67 |
![]() s elektronovou konfigurací neonu, chlor doplněním jednoho elektronu do podslupky 3p vytvoří iont
s elektronovou konfigurací neonu, chlor doplněním jednoho elektronu do podslupky 3p vytvoří iont ![]() s elektronovou konfigurací argonu. Oba ionty se pak chemicky váží přitažlivými elektrostatickými silami v molekulu NaCl. Iontově vázaná molekula může ve vodném roztoku opět disociovat, tj. rozložit se na kladný a záporný iont a vytvořit elektrolyt.
s elektronovou konfigurací argonu. Oba ionty se pak chemicky váží přitažlivými elektrostatickými silami v molekulu NaCl. Iontově vázaná molekula může ve vodném roztoku opět disociovat, tj. rozložit se na kladný a záporný iont a vytvořit elektrolyt.
