Encyklopedie fyziky |
|
Voltampérová charakteristika elektrolytického vodiče
Vložíme-li do vaničky s roztokem ![]() dvě měděné elektrody, zapojíme obvod a budeme postupně zvyšovat napětí, zjistíme, že proud je přímo úměrný napětí a tedy platí Ohmův zákon (viz obr. 105a). Pokud elektrody od sebe oddálíme nebo snížíme hladinu elektrolytu v nádobě, proud se zmenší. Odpor elektrolytického vodiče tedy splňuje vztah
dvě měděné elektrody, zapojíme obvod a budeme postupně zvyšovat napětí, zjistíme, že proud je přímo úměrný napětí a tedy platí Ohmův zákon (viz obr. 105a). Pokud elektrody od sebe oddálíme nebo snížíme hladinu elektrolytu v nádobě, proud se zmenší. Odpor elektrolytického vodiče tedy splňuje vztah ![]() , kde l je jeho délka a S příčný průřez. Měrný elektrický odpor
, kde l je jeho délka a S příčný průřez. Měrný elektrický odpor ![]() elektrolytu s rostoucí teplotou klesá, neboť se zmenšuje vnitřní tření brzdící pohyb iontů v elektrolytu.
elektrolytu s rostoucí teplotou klesá, neboť se zmenšuje vnitřní tření brzdící pohyb iontů v elektrolytu.
Tření se zmenšuje v důsledku poklesu hustoty elektrolytu.
Odlišný výsledek zaznamenáme s roztokem ![]() a platinovými (nebo uhlíkovými) elektrodami. Při malém napětí vznikne nepatrný proud, který za krátkou dobu opět zanikne. Při pomalém zvětšování napětí se tento jev opakuje, dokud nepřekročíme tzv. rozkladné napětí
a platinovými (nebo uhlíkovými) elektrodami. Při malém napětí vznikne nepatrný proud, který za krátkou dobu opět zanikne. Při pomalém zvětšování napětí se tento jev opakuje, dokud nepřekročíme tzv. rozkladné napětí ![]() (viz obr. 105b). Potom proud v závislosti na napětí roste lineárně a elektrolýza probíhá již standardně. Závislost proudu na napětí je popsána vztahem
(viz obr. 105b). Potom proud v závislosti na napětí roste lineárně a elektrolýza probíhá již standardně. Závislost proudu na napětí je popsána vztahem ![]() , který se odlišuje od Ohmova zákona.
, který se odlišuje od Ohmova zákona.
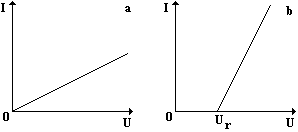 |
| Obr. 105 |
Příčinou vzniku rozkladného napětí ![]() jsou děje probíhající na elektrodách. Při ponoření kovové elektrody do elektrolytu dochází k reakci, při níž část iontů kovu přechází do elektrolytu a na elektrodě převládne záporný náboj elektronů (ponoření Zn elektrody do roztoku
jsou děje probíhající na elektrodách. Při ponoření kovové elektrody do elektrolytu dochází k reakci, při níž část iontů kovu přechází do elektrolytu a na elektrodě převládne záporný náboj elektronů (ponoření Zn elektrody do roztoku ![]() , …) nebo se část kationtů z elektrolytu připojí ke krystalické mříži elektrody, která se nabije kladně (ponoření Cu elektrody do
, …) nebo se část kationtů z elektrolytu připojí ke krystalické mříži elektrody, která se nabije kladně (ponoření Cu elektrody do ![]() , …). Na rozhraní kovu a elektrolytu vzniká elektrická dvojvrstva s určitým elektromotorickým napětím. V případě měděných elektrod v roztoku
, …). Na rozhraní kovu a elektrolytu vzniká elektrická dvojvrstva s určitým elektromotorickým napětím. V případě měděných elektrod v roztoku ![]() zůstávají elektrody během elektrolýzy stejné a elektromotorická napětí obou dvojvrstev se navenek ruší. V případě uhlíkových elektrod v roztoku
zůstávají elektrody během elektrolýzy stejné a elektromotorická napětí obou dvojvrstev se navenek ruší. V případě uhlíkových elektrod v roztoku ![]() se katoda pokrývá bublinkami vodíku a anoda bublinkami kyslíku. Vznikají tedy dvě různé dvojvrstvy, jejichž elektromotorická napětí jsou různá a jejichž rozdíl se navenek projevuje vznikem rozkladného napětí
se katoda pokrývá bublinkami vodíku a anoda bublinkami kyslíku. Vznikají tedy dvě různé dvojvrstvy, jejichž elektromotorická napětí jsou různá a jejichž rozdíl se navenek projevuje vznikem rozkladného napětí ![]() . Říkáme, že elektrody se polarizují a vzniká na nich polarizační napětí opačně orientované než elektromotorické napětí připojeného vnějšího zdroje.
. Říkáme, že elektrody se polarizují a vzniká na nich polarizační napětí opačně orientované než elektromotorické napětí připojeného vnějšího zdroje.
Vytvoření elektrické dvojvrstvy na rozhraní kov - elektrolyt se využívá v galvanických článcích.
-
3.1 |
ELEKTRICKÝ NÁBOJ A ELEKTRICKÉ POLE
3.1.1 | Elektrický náboj a jeho vlastnosti
3.1.2 | Elektrostatické silové působení bodových elektrických nábojů, Coulombův zákon
3.1.3 | Elektrické pole, elektrická intenzita
3.1.4 | Práce v elektrostatickém poli, elektrické napětí
3.1.5 | Potenciální energie elektrostatického pole, elektrický potenciál
3.1.6 | Elektrostatické pole nabitého vodivého tělesa ve vakuu
3.1.7 | Vodič a izolant v elektrostatickém poli
3.1.7.1 | Vodič
3.1.7.2 | Izolant
3.1.7.3 | ***Elektrická pevnost dielektrika
3.1.8 | ***Elektrická indukce
3.1.9 | Kapacita vodiče, kondenzátor
3.1.9.1 | Deskový kondenzátor
3.1.9.2 | Válcový kondenzátor
3.1.9.3 | Kulový kondenzátor
3.1.10 | Kondenzátory - užití, spojování, energie
3.1.10.1 | Kondenzátory v praxi
3.1.10.2 | Spojování kondenzátorů
3.1.10.3 | Energie kondenzátoru
3.1.11 | ***Elektrostatické jevy v praxi
3.1.11.1 | Pohyb nabité částice v elektrostatickém poli
3.1.11.1.1 | Fyzikální principy
3.1.11.1.2 | Praktická realizace
3.1.11.2 | Elektrostatické jevy v průmyslu
3.2 | VZNIK ELEKTRICKÉHO PROUDU
3.2.1 | Elektrický proud jako děj a jako fyzikální veličina
3.2.2 | Elektrický zdroj, přeměny energie v jednoduchém obvodu
3.2.3 | Termoelektrické články
3.2.3.1 | Seebeckův jev
3.2.3.2 | Peltierův jev
3.2.3.3 | Thomsonův jev
3.3 | ELEKTRICKÝ PROUD V KOVECH
3.3.1 | Elektrický odpor vodiče, Ohmův zákon pro část obvodu
3.3.2 | Závislost odporu kovového vodiče na teplotě
3.3.3 | ***Hodnoty rezistorů a jejich barevné značení
3.3.4 | Kovový vodič z hlediska vnitřní struktury
3.3.4.1 | Vedení elektrického proudu
3.3.4.2 | ***Vysvětlení závislosti odporu kovu na teplotě
3.3.5 | Spojování rezistorů
3.3.5.1 | Sériové spojení rezistorů
3.3.5.2 | Paralelní spojení rezistorů
3.3.5.3 | Přeměna (transfigurace) trojúhelníka na hvězdu
3.3.5.4 | Přeměna (transfigurace) hvězdy a na trojúhelník
3.3.6 | Zatěžovací charakteristika zdroje, Ohmův zákon pro uzavřený obvod
3.3.7 | Sériové a paralelní obvody
3.3.7.1 | Regulace proudu a napětí reostatem
3.3.7.2 | Regulace proudu a napětí potenciometrem
3.3.7.3 | Dělič napětí
3.3.7.4 | Konstrukce a změna rozsahu ampérmetru a voltmetru
3.3.7.4.1 | Voltmetr
3.3.7.4.2 | Ampérmetr
3.3.7.5 | Měření odporu rezistoru
3.3.7.6 | Wheatstoneův můstek
3.3.8 | Kirchhoffovy zákony
3.3.9 | Elektrická práce a výkon v obvodu stejnosměrného proudu
3.4 | ELEKTRICKÝ PROUD V POLOVODIČÍCH
3.4.1 | Polovodiče
3.4.2 | Vznik a vedení elektrického proudu v polovodičích
3.4.2.1 | Vlastní polovodiče
3.4.2.2 | Příměsové polovodiče
3.4.3 | Přechod PN
3.4.3.1 | Fyzikální podstata přechodu PN
3.4.3.2 | Osvětlení přechodu
3.4.3.3 | ***Zapojení přechodu v závěrném směru
3.4.4 | Polovodičové součástky
3.4.4.1 | Termistor
3.4.4.2 | Fotorezistor
3.4.4.3 | Tenzometrické součástky
3.4.4.4 | Dioda
3.4.4.4.1 | Usměrňující dioda
3.4.4.4.2 | Zenerova (stabilizační) dioda
3.4.4.5 | Fotodioda
3.4.4.6 | LED
3.5 | ELEKTRICKÝ PROUD V KAPALINÁCH
3.5.1 | Elektrolyt, elektrolýza
3.5.2 | Faradayovy zákony elektrolýzy
3.5.3 | Elektrická dvojvrstva a standardní elektrodový potenciál
3.5.3.1 | Interakce kovu a roztoku
3.5.3.2 | Beketovova řada kovů
3.5.4 | Voltampérová charakteristika elektrolytického vodiče
3.5.5 | Galvanické články a akumulátory
3.5.5.1 | Voltův článek
3.5.5.2 | Daniellův článek
3.5.5.3 | Leclancheův článek
3.5.5.4 | Olověný akumulátor
3.5.5.5 | Lithiové akumulátory
3.5.6 | Polarografie
3.6 | ELEKTRICKÝ PROUD V PLYNECH A VE VAKUU
3.6.1 | Nesamostatný a samostatný výboj v plynu
3.6.2 | Samostatný výboj v plynu za atmosférického a za sníženého tlaku
3.6.3 | Katodové a kanálové záření, obrazovka
3.7 | STACIONÁRNÍ MAGNETICKÉ POLE
3.7.1 | Základní poznatky o magnetickém poli
3.7.2 | Magnetické pole vodiče s proudem
3.7.3 | Magnetická síla
3.7.4 | ***Vysvětlení vzniku magnetického pole v okolí vodiče s proudem
3.7.5 | Magnetická indukce
3.7.6 | Magnetické pole rovnoběžných vodičů s proudem
3.7.7 | Magnetické pole cívky
3.7.7.1 | ***„Speciální“ cívky
3.7.8 | Částice s nábojem v magnetickém poli
3.7.9 | ***Hallův jev
3.7.10 | Magnetické vlastnosti látek
3.7.11 | ***Magnetická hystereze
3.7.12 | Magnetické materiály v praxi
3.7.12.1 | Elektromagnetické relé
3.7.12.2 | Magnetický záznam signálu
3.7.12.3 | Měřící přístroj s otočnou cívkou
3.8 | NESTACIONÁRNÍ MAGNETICKÉ POLE
3.8.1 | Elektromagnetická indukce
3.8.2 | Magnetický indukční tok
3.8.3 | Faradayův zákon elektromagnetické indukce
3.8.3.1 | ***Odvození Faradayova zákona elektromagnetické indukce
3.8.4 | Indukovaný proud
3.8.5 | Vlastní indukce
3.8.6 | Přechodný děj
3.8.7 | Energie magnetického pole cívky
3.9 | STŘÍDAVÝ PROUD
3.9.1 | Zdroje střídavého proudu
3.9.2 | Obvody střídavého proudu
3.9.2.1 | Obvod s rezistorem
3.9.2.2 | Obvod s cívkou
3.9.2.3 | Obvod s kondenzátorem
3.9.2.4 | Složený obvod
3.9.2.4.1 | Sériový RLC obvod
3.9.2.4.2 | Sériový RLC obvod - popis pomocí komplexních čísel
3.9.2.4.3 | Paralelní RLC obvod
3.9.2.4.4 | Derivační a integrační články
3.9.2.4.4.1 | Derivační článek
3.9.2.4.4.2 | Integrační článek
3.9.3 | Výkon střídavého proudu
3.9.3.1 | Obvod s odporem
3.9.3.2 | Obvod s impedancí
3.10 | STŘÍDAVÝ PROUD V ENERGETICE
3.10.1 | Základní rozbor
3.10.2 | Generátor střídavého proudu
3.10.3 | Trojfázová soustava střídavého napětí
3.10.4 | ***Zásuvka a zástrčka
3.10.5 | ***Pojistky a jističe
3.10.5.1 | Pojistky
3.10.5.2 | Jističe
3.10.6 | Elektromotor na trojfázový proud
3.10.7 | Transformátor
3.10.7.1 | Jednofázové transformátory
3.10.7.2 | Trojfázové transformátory
3.10.8 | Přenos elektrické energie
3.10.9 | ***Ochrana před úrazem elektrickým proudem
3.11 | FYZIKÁLNÍ ZÁKLADY ELEKTRONIKY
3.11.1 | Usměrňovač
3.11.2 | Tranzistor
3.11.2.1 | Bipolární tranzistory
3.11.2.1.1 | Zapojení tranzistorů
3.11.2.1.1.1 | ***Zapojení se společnou bází
3.11.2.1.1.2 | Zapojení se společným emitorem
3.11.2.1.1.3 | Zapojení se společným kolektorem
3.11.2.1.2 | Výroba tranzistorů
3.11.2.1.3 | TFT (Thin Film Transistor)
3.11.2.2 | Unipolární tranzistory
3.11.2.2.1 | MOSFET
3.11.2.2.1.1 | Popis a použití
3.11.2.2.1.2 | Princip činnosti tranzistoru s indukovaným kanálem
3.11.2.2.1.3 | Princip činnosti tranzistoru se zabudovaným kanálem
3.11.2.3 | ***„Speciální“ tranzistory
3.11.2.3.1 | Fototranzistor
3.11.2.3.2 | Piezotranzistor
3.11.2.3.3 | Zesilovač
3.11.2.3.4 | ***Spínač
3.11.2.3.5 | Integrované obvody
3.12 | ELEKTROMAGNETICKÉ KMITÁNÍ A VLNĚNÍ
3.12.1 | Základní pojmy
3.12.2 | Elektromagnetický oscilátor
3.12.3 | Perioda kmitání elektromagnetického oscilátoru
3.12.4 | Nucené kmitání elektromagnetického oscilátoru
3.12.5 | Vznik elektromagnetického vlnění
3.12.6 | Elektromagnetická vlna
3.12.7 | Elektromagnetický dipól
3.12.8 | Vlastnosti elektromagnetického vlnění
3.12.8.1 | Polarizace
3.12.8.2 | Odraz a ohyb
3.12.8.3 | Interference
3.12.8.4 | Vliv prostředí na vlnovou délku
3.12.8.5 | Šíření elektromagnetického vlnění
3.12.9 | ***Druhy elektromagnetického vlnění
3.12.10 | Elektromagnetická interakce
3.12.10.1 | ***Maxwellovy rovnice
3.13 | PŘENOS INFORMACÍ ELEKTROMAGNETICKÝM VLNĚNÍM
3.13.1 | Výchozí situace
3.13.2 | Sdělovací soustava
3.13.3 | Vysílač
3.13.4 | Přijímač
3.13.5 | Princip televize
3.14 | ELEKTROAKUSTIKA
3.14.1 | Elektroakustické měniče
3.14.1.1 | Mikrofony
3.14.1.1.1 | Základní vlastnosti mikrofonů
3.14.1.1.1.1 | Citlivost mikrofonu
3.14.1.1.1.2 | Impedance mikrofonu
3.14.1.1.1.3 | Šum mikrofonu
3.14.1.1.1.4 | Frekvenční charakteristika mikrofonu
3.14.1.1.1.5 | Směrová charakteristika mikrofonu
3.14.1.1.2 | Odporový (uhlíkový) mikrofon
3.14.1.1.3 | Elektrodynamický mikrofon
3.14.1.1.4 | Elektromagnetický mikrofon
3.14.1.1.5 | Krystalový mikrofon
3.14.1.1.6 | Elektrostatický mikrofon
3.14.1.2 | Zesilovače
3.14.1.3 | Reproduktory
3.14.1.3.1 | Základní vlastnosti reproduktorů
3.14.1.3.1.1 | Frekvenční charakteristika reproduktoru
3.14.1.3.1.2 | Směrová charakteristika reproduktoru
3.14.1.3.1.3 | Rezonanční frekvence reproduktoru
3.14.1.3.1.4 | Zkreslení reproduktoru
3.14.1.3.1.5 | Zatížitelnost reproduktoru
3.14.1.3.1.6 | Jmenovitá impedance reproduktoru
3.14.1.3.1.7 | Účinnost reproduktoru
3.14.1.3.1.8 | Charakteristická citlivost reproduktoru
3.14.1.3.2 | Elektrodynamický reprodukor
3.14.1.3.3 | Piezoelektrický reproduktor
3.14.1.3.4 | Elektrostatický reproduktor
3.14.1.3.5 | Tlakové reproduktory
3.14.1.3.6 | Reproduktorové soustavy
3.14.2 | Kompaktní disk (CD)
3.14.2.1 | Princip záznamu a reprodukce zvuku
3.14.2.2 | Průmyslová výroba CD
3.14.3 | Gramofon
3.14.3.1 | Historie vzniku gramofonu
3.14.3.2 | Současný gramofon
3.14.3.3 | Přenoska gramofonu
3.14.3.4 | Výroba gramofonových desek
3.14.3.5 | Druhy gramofonových desek
3.15 | DODATKY
3.15.1 | Piezoelektrický jev
3.15.1.1 | Vysvětlení jevu
3.15.1.2 | Druhy piezoelektrických látek
3.15.1.2.1 | Krystalické piezoelektrické látky
3.15.1.2.2 | Piezoelektrická keramika
3.15.2 | Kapalné krystaly
3.15.3 | Technologie DMD
3.15.4 | Technologie LCoS
3.15.5 | Supravodivost
3.15.5.1 | Meissnerův jev
3.15.5.2 | Supravodič jako zdroj elektromagnetického pole
3.15.5.3 | Druhy supravodičů
3.15.5.4 | Využití supravodičů
3.15.5.5 | Podstata supravodivosti
3.15.6 | Supratekutost
Partnerský web Online Domain Tools