Rozdělení molekul plynu podle rychlostí
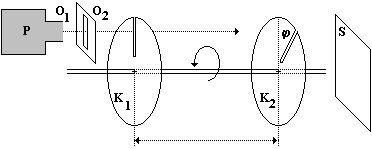
Všechny molekuly plynu, který je v rovnovážném stavu nemají v určitém okamžiku stejnou rychlost, což je dáno vzájemnými srážkami molekul. Při nich dochází ke změně velikosti i směru rychlosti. Velikost rychlostí molekul plynu lze zjistit např. Lammetrovým pokusem (viz obr. 19). Dva kotouče ![]() a
a ![]() s radiální štěrbinou jsou umístěny ve vakuu ve vzájemné vzdálenosti d a otáčejí se na společné hřídeli stálou úhlovou rychlostí
s radiální štěrbinou jsou umístěny ve vakuu ve vzájemné vzdálenosti d a otáčejí se na společné hřídeli stálou úhlovou rychlostí ![]() . Štěrbiny jsou vůči sobě pootočeny o úhel
. Štěrbiny jsou vůči sobě pootočeny o úhel ![]() . V elektricky vyhřívané peci P jsou páry rtuti. Po průchodu nehybnými štěrbinami
. V elektricky vyhřívané peci P jsou páry rtuti. Po průchodu nehybnými štěrbinami ![]() a
a ![]() vytvářejí molekuly rtuti úzký molekulový svazek, v němž se vyskytují molekuly pohybující se různými rychlostmi. Oběma rotujícími štěrbinami však projdou jen ty molekuly, které urazí vzdálenost d za stejný čas, za který se druhá štěrbina otočí o úhel
vytvářejí molekuly rtuti úzký molekulový svazek, v němž se vyskytují molekuly pohybující se různými rychlostmi. Oběma rotujícími štěrbinami však projdou jen ty molekuly, které urazí vzdálenost d za stejný čas, za který se druhá štěrbina otočí o úhel ![]() . Protože platí
. Protože platí ![]() a
a ![]() , dostáváme
, dostáváme ![]() .
.
 |  |
| Obr. 19 | Obr. 20 |
Změnou parametrů d, ![]() nebo
nebo ![]() lze z molekulového paprsku postupně vybrat molekuly, jejichž rychlost leží v určitém intervalu
lze z molekulového paprsku postupně vybrat molekuly, jejichž rychlost leží v určitém intervalu ![]() . Z hmotnosti náletů na stínítko S lze určit počet těchto molekul. Tímto způsobem je možné určit rozdělení molekul podle (velikosti) rychlostí.
. Z hmotnosti náletů na stínítko S lze určit počet těchto molekul. Tímto způsobem je možné určit rozdělení molekul podle (velikosti) rychlostí.
Rozdělení molekul podle rychlostí lze znázornit:
1. tabulkou - zapisujeme intervaly rychlostí ![]() a k nim příslušné střední relativní četnosti molekul
a k nim příslušné střední relativní četnosti molekul ![]() , jejichž rychlost leží v uvažovaném intervalu rychlostí
, jejichž rychlost leží v uvažovaném intervalu rychlostí
2. histogramem
3. graf rozdělení molekul podle rychlostí - získáme ho z histogramu, snižujeme-li postupně ![]() , tj.
, tj. ![]() .
.
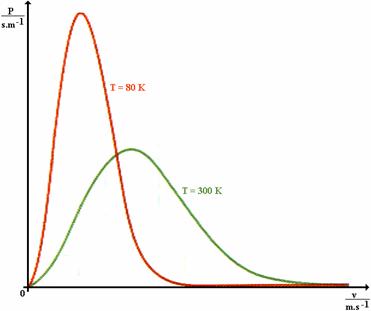
Rozdělení molekul podle rychlostí závisí na teplotě plynu (viz obr. 20): při vyšší teplotě je relativní četnost molekul s malými rychlostmi menší a relativní četnost molekul s velkými rychlostmi větší. Zákon rozdělení molekul podle rychlostí odvodil jako první skotský fyzik J. C. Maxwell, který se tímto problémem zabýval od roku 1852.
Na obr. 20 je v grafu na svislé ose vynesena veličina ![]() , která se nazývá rozdělovací funkce, která má tvar:
, která se nazývá rozdělovací funkce, která má tvar: ![]() . Její jednotka je taková, že součin
. Její jednotka je taková, že součin ![]() je bezrozměrový. Tento součin přitom udává relativní četnost molekul s velikostmi rychlostí v intervalu
je bezrozměrový. Tento součin přitom udává relativní četnost molekul s velikostmi rychlostí v intervalu ![]() . Číselná hodnota plochy pod křivkou rozdělovací funkce z obr. 20 na intervalu
. Číselná hodnota plochy pod křivkou rozdělovací funkce z obr. 20 na intervalu ![]() udává relativní počet molekul, jejichž velikosti rychlostí leží v uvažovaném intervalu
udává relativní počet molekul, jejichž velikosti rychlostí leží v uvažovaném intervalu ![]() .
.
Představíme-li si na svislé ose místo veličiny P počet částic, které se pohybují danou rychlostí, nebude to sice zcela přesné, ale pro pochopení grafu postačující.
Multimedialní obsah
 Audio č.1
Audio č.1
|
[331.53 kB] | [Uložit] |  Prezentace č.1
Prezentace č.1
|
[395.5 kB] | [Uložit] |