Vazby v krystalech
Mezi částicemi pevné látky vždy působí vazebné síly, které plní stejnou funkci jako síly mezi atomy v osamocené molekule: váží k sobě částice, z nichž se látka (krystalová mřížka) skládá. U pevných látek se jedná o tyto vazby:
1. iontová - převažuje u krystalů alkalických halogenidů (NaCl, KBr, CsCl, …) a krystalů oxidů alkalických zemin (CaO, …). Jedná se o vazbu mezi elektronegativním a elektropozitivním prvkem. Vazba se uskutečňuje pomocí elektronu. Tento elektron přitom jeden atom (většinou atom alkalických kovů - Li, Na, K, Rb, Cs, Fr) uvolní, čímž se z něj stane kationt, a druhý atom (halogeny - F, Cl, Br, I, At) přijme; tím se z něj stane aniont. Takto vzniklé ionty se začnou přitahovat elektrostatickou silou (viz schematicky obr. 48); tato síla je tedy podstatou iontové vazby.
Iontové krystaly jsou značně tvrdé a mají poměrně vysokou teplotu tání. Jsou křehké a štěpné podél rovin kolmých na hrany základní buňky. Za běžných teplot jsou elektrickými izolanty, při vyšších teplotách se stávají elektricky vodivými. Pro viditelné světlo jsou většinou propustné.
2. vodíková (vodíkový můstek) - spojuje např. krystaly ledu vody, často se vyskytuje v organických látkách.
3. kovová - atomy kovových prvků (např. Cu, Fe, Al, …) mají jeden, dva nebo maximálně tři valenční elektrony. Tyto elektrony jsou k atomovému jádru velmi slabě vázány, a proto se snadno uvolňují. K dalšímu atomu se již neváží, ale jsou téměř volné a pohybují se chaotickým pohybem mezi kationy kovových atomů (viz obr. 49).
Kationty vznikly právě výše popsaným odtržením elektronů od původně elektricky neutrálních atomů.
Volné elektrony tak vytvářejí tzv. elektronový plyn. Tyto pohybující se elektrony jednak odstiňují elektrostatické silové působení kladných iontů mřížky a současně zprostředkovávají elektrostatickou přitažlivou sílu, která drží atomy pohromadě.
Kovové krystaly mají velmi dobrou tepelnou a elektrickou vodivost, povrchový lesk a v silnějších vrstvách jsou neprůhledné. Nejsou štěpné a některé se vyznačují dobrou kujností a tažností.
4. kovalentní - podstatou vazby je tzv. sdílení elektronů sousedními atomy (viz obr. 50). Dva kovalentně vázané atomy přispívají každý nejméně jedním elektronem k vazbě; tyto elektrony pak patří oběma atomům. Vazba je směrová (uskutečňuje se pouze pod určitými úhly) a nasycená (je nasycená mocenstvím vázaných atomů).
V přírodě je velmi rozšířená - váží se jí atomy nekovových prvků samy se sebou v molekuly (H2 , Cl2 , O2, …), stejně jako mezi sebou (CH4, H2O, HNO3, …); též ale diamant, krystal křemíku, … Kovalentní (atomové) krystaly jsou tvrdé, mají vysokou teplotu tání, jsou nerozpustné v běžných rozpouštědlech a patří mezi elektrické izolanty nebo polovodiče. Při vzniku polymerů umožňuje tato vazba tvorbu dlouhých řetězců atomů a molekul.
5. van der Waalsova - vazba slabá. Typická pro krystaly inertních prvků, které jsou stabilní jen za velmi nízkých teplot. Vyskytuje se také u I, Cl, O, H za nízkých teplot a u organických sloučenin. Jedná se o vazbu elektrické povahy.
Mají-li krystaly velkou relativní hmotnost, mohou být v pevném skupenství i za pokojové teploty (parafin, …). Krystaly s touto vazbou se nazývají molekulové krystaly - měkké krystaly s nízkou teplotou tání.
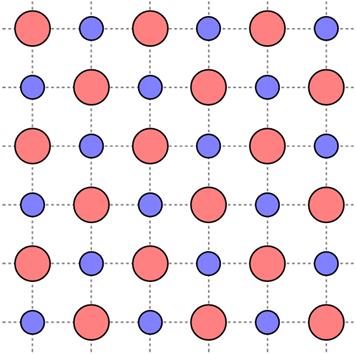 | 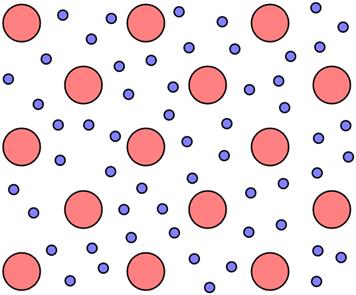 |
| Obr. 48 | Obr. 49 |
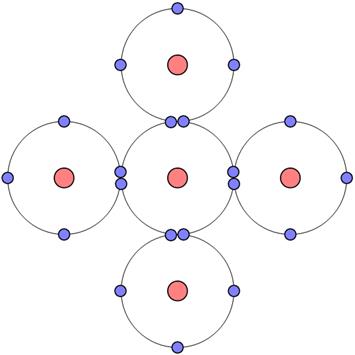 |
| Obr. 50 |
V reálných krystalech se uplatňuje více typů vazeb. U grafitu jsou atomy uhlíku vázány kovalentními vazbami do pravidelných šestiúhelníků. Jednotlivé vrstvy pak jsou vázány slabou van der Waalsovou vazbou, což má za následek, že se grafit (tuha) lehce otírá. Naproti tomu karbidy, nitridy a boridy (většinou uměle vyráběné) jsou mimořádně tvrdé, těžko tavitelné a chemicky dobře odolné, neboť se v nich uplatňuje kombinace vazby kovové a kovalentní. Uvedenými vlastnostmi jsou tyto látky vhodné k výrobě břitů obráběcích strojů, užívají se v raketové technice a chemickém provozu.