Fázový diagram
Všechna tři skupenství, jejich rovnovážné stavy a jednotlivé změny skupenství lze znázornit a popsat v tzv. fázovém diagramu dané látky. Fázový diagram je zobrazen na obr. 71 a se skládá ze tří křivek ![]() (křivka syté páry),
(křivka syté páry), ![]() (křivka tání) a
(křivka tání) a ![]() (křivka sublimace).
(křivka sublimace).
Body křivky tání ![]() znázorňují různé rovnovážné stavy, v nichž se vyskytuje pevné a kapalné skupenství uvažované látky. Zároveň ukazuje graf závislosti teploty tání na vnějším tlaku. Začíná v bodě A (jako křivka syté páry), v němž je pevné a kapalné skupenství téže látky ještě v rovnováze. Křivka není ukončena - nejsou známy experimenty, které by na její konec ukazovaly.
znázorňují různé rovnovážné stavy, v nichž se vyskytuje pevné a kapalné skupenství uvažované látky. Zároveň ukazuje graf závislosti teploty tání na vnějším tlaku. Začíná v bodě A (jako křivka syté páry), v němž je pevné a kapalné skupenství téže látky ještě v rovnováze. Křivka není ukončena - nejsou známy experimenty, které by na její konec ukazovaly.
Každý bod sublimační křivky ![]() znázorňuje stav látky, při němž jsou vede sebe v rovnovážném stavu pevná látka a její sytá pára. Křivka směřuje do počátku soustavy souřadnic a končí v bodě A.
znázorňuje stav látky, při němž jsou vede sebe v rovnovážném stavu pevná látka a její sytá pára. Křivka směřuje do počátku soustavy souřadnic a končí v bodě A.
Všechny tři křivky se stýkají v jednom bodě - v bodě A, který se nazývá trojný bod a ve fázovém diagramu znázorňuje rovnovážný stav pevného, kapalného a plynného skupenství téže látky. Např. při teplotě ![]() a tlaku
a tlaku ![]() existují v rovnovážném stavu současně led, voda a sytá vodní pára. Teplota trojného bodu vody je základní teplotou termodynamické teplotní stupnice.
existují v rovnovážném stavu současně led, voda a sytá vodní pára. Teplota trojného bodu vody je základní teplotou termodynamické teplotní stupnice.
Křivky ![]() ,
, ![]() a
a ![]() rozdělují rovinu fázového diagramu na tři oblasti - I., II., III.:
rozdělují rovinu fázového diagramu na tři oblasti - I., II., III.:
1. oblast I. znázorňuje stav látky v pevném skupenství
2. oblast II. znázorňuje stav látky v kapalném skupenství
3. oblast III. znázorňují různé rovnovážné stavy plynného skupenství, které má nižší tlak než sytá pára téže teploty. Toto plynné skupenství nazýváme přehřátá pára.
Přehřátá pára může vzniknout ze syté páry dvěma základními způsoby:
1. zvětšením objemu syté páry bez přítomnosti kapaliny (což je spojeno s poklesem tlaku)
2. zahříváním syté páry bez přítomnosti kapaliny
Přehřátá pára je tedy pára, která má nižší tlak a hustotu než sytá pára téže teploty. Přehřátou páru lze považovat za ideální plyn tím spíše, čím více se její stav liší od stavu syté páry.
Přechod z jedné oblasti do druhé ve fázovém diagramu protnutím jedné z křivek ![]() ,
, ![]() nebo
nebo ![]() představuje vždy změnu skupenství, během níž se vytvoří rozhraní mezi jednotlivými skupenstvími. Na obr. 71 je zobrazen bod P, který představuje rovnovážný stav soustavy při teplotě vyšší než je teplota kritická
představuje vždy změnu skupenství, během níž se vytvoří rozhraní mezi jednotlivými skupenstvími. Na obr. 71 je zobrazen bod P, který představuje rovnovážný stav soustavy při teplotě vyšší než je teplota kritická ![]() . Má-li být látka v tomto stavu zkapalněna, musí být nejprve ochlazena (většinou adiabatickou expanzí) na teplotu nižší, než je teplota kritická, a pak může teprve proběhnout komprese.
. Má-li být látka v tomto stavu zkapalněna, musí být nejprve ochlazena (většinou adiabatickou expanzí) na teplotu nižší, než je teplota kritická, a pak může teprve proběhnout komprese.
Kromě změny skupenství, kdy je tato změna přímo „vidět“, lze ale také uskutečnit takový přechod z plynného skupenství v kapalné (a zpět), během něhož se nikdy nevytvoří rozhraní mezi plynem a kapalinou a látka je stále stejnorodá. Tento děj lze realizovat tak, že látku, která je ve stavu P, nejprve izotermicky stlačíme tak, až látka dosáhne tlaku vyššího než je tlak kritický. Následuje izobarické ochlazení, během něhož nelze rozhodnout, v jakém skupenství se látka nachází (je stále stejnorodá), ale stále se zvyšuje hustota látky. Izotermickým přechodem dosáhneme snížení tlaku kapaliny pod hodnotu kritického tlaku.
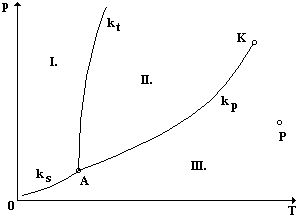 |
| Obr. 71 |