Adiabatický děj
Při adiabatickém ději neprobíhá tepelná výměna mezi plynem a okolím a proto tedy je ![]() . První termodynamický zákon pak můžeme psát ve tvaru
. První termodynamický zákon pak můžeme psát ve tvaru ![]() . Při adiabatickém stlačení plynu v nádobě se působením vnější síly na píst koná práce, teplota plynu a jeho vnitřní energie se zvětšuje. Při adiabatickém rozpínání koná práci plyn, teplota plynu i jeho vnitřní energie se zmenšuje.
. Při adiabatickém stlačení plynu v nádobě se působením vnější síly na píst koná práce, teplota plynu a jeho vnitřní energie se zvětšuje. Při adiabatickém rozpínání koná práci plyn, teplota plynu i jeho vnitřní energie se zmenšuje.
Je-li píst v klidu, velikost rychlosti molekul se po odrazu od stěn nádoby nemění, a proto teplota plynu zůstává stálá. Při zmenšování objemu plynu posouváním pístu, se molekuly od něho odrážejí s větší rychlostí, což má za následek vzrůst teploty plynu. Při rozpínání plynu je píst plynem z nádoby vytlačován a molekuly se od něho odrážejí s menší rychlostí. Tím se snižuje teplota plynu i jeho vnitřní energie.
Pro adiabatický děj s ideálním plynem stálé hmotnosti platí Poissonův zákon: ![]() , kde
, kde ![]() je Poissonova konstanta. Vzhledem k tomu, že
je Poissonova konstanta. Vzhledem k tomu, že ![]() , je
, je ![]() . Poissonova konstanta závisí na druhu plynu, ale přibližně platí toto:
. Poissonova konstanta závisí na druhu plynu, ale přibližně platí toto:
1. pro plyn s jednoatomovými molekulami je ![]()
2. pro plyn s dvouatomovými molekulami je ![]()
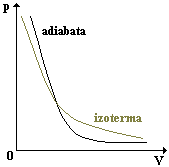 |
| Obr. 25 |
Graf vyjadřující závislost tlaku ideálního plynu stálé hmotnosti jako funkci jeho objemu se nazývá adiabata. Adiabata klesá vždy strměji než izoterma (viz obr. 25).
… to proto, že izoterma má rovnici ![]() , zatímco adiabata
, zatímco adiabata ![]() , kde
, kde ![]() !
!
V praxi lze adiabatické komprese nebo adiabatické expanze dosáhnout rychlou změnou objemu plynu v krátké době, při níž plyn nestačí přijmout nebo odevzdat svému okolí teplo. Např. adiabatické expanze se používá k dosažení nízkých teplot, adiabatická komprese se používá u vznětových motorů: adiabatickou kompresí se zvýší teplota vzduchu na zápalnou teplotu nafty, která se po vstříknutí do tohoto vzduchu sama vznítí.
Za adiabatické lze tedy považovat ty děje, které probíhají natolik rychle, že se nestíhá vyrovnávat teplota plynu s teplotou okolí! Např. únik plynu z bombičky na sifonovou láhev, plnění zapalovače z bombičky, …