Povrchová vrstva kapaliny
Položíme-li na volný povrch vody např. žiletku, desetník, jehlu, … pozorujeme dvě věci: volný povrch kapaliny se pod tělesem prohne a dané těleso se nepotopí, ačkoliv jeho hustota je větší než hustota vody. Kapka, která se vytváří na konci vodovodního kohoutku, postupně roste, pak se vytvoří krček a kapka se odtrhne (kapka se jeví jako pružný balónek, v němž je voda) (vodoměrka se pohybuje po hladině, stan v dešti nepromokne, …). Tyto pokusy ukazují, že volný povrch kapaliny se chová jako tenká pružná blána.
Molekuly kapaliny na sebe vzájemně působí přitažlivými silami, jejichž velikost s rostoucí vzdáleností molekul klesá. Kolem každé molekuly si lze představit kouli (sféru molekulového působení) o takovém poloměru ![]() , aby síly, jimiž na danou molekulu působí ostatní molekuly v této kouli neležící, byly zanedbatelné. Poloměr této sféry je řádově 1 nm (tj. několik mezimolekulových vzdáleností).
, aby síly, jimiž na danou molekulu působí ostatní molekuly v této kouli neležící, byly zanedbatelné. Poloměr této sféry je řádově 1 nm (tj. několik mezimolekulových vzdáleností).
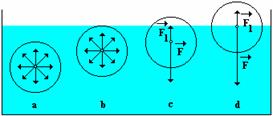 |
| Obr. 58 |
Je-li molekula i její sféra molekulového působení uvnitř kapaliny, pak výslednice přitažlivých sil, jimiž molekuly v této sféře působí na uvažovanou molekulu, je nulová (viz obr. 58 a, b). Na molekulu, jejíž vzdálenost od volného povrchu kapaliny je menší než ![]() , působí výslednice
, působí výslednice ![]() přitažlivých sil, jimiž působí molekuly kapaliny ve sféře uvažované molekuly na tuto molekulu, kolmo k volnému povrchu kapaliny a má směr dovnitř kapaliny. Molekuly plynu (který je nad volným povrchem kapaliny) v horní části sféry působí na molekulu v jejím středu výslednou přitažlivou silou
přitažlivých sil, jimiž působí molekuly kapaliny ve sféře uvažované molekuly na tuto molekulu, kolmo k volnému povrchu kapaliny a má směr dovnitř kapaliny. Molekuly plynu (který je nad volným povrchem kapaliny) v horní části sféry působí na molekulu v jejím středu výslednou přitažlivou silou ![]() opačného směru, než je směr síly
opačného směru, než je směr síly ![]() . Vzhledem k tomu, že
. Vzhledem k tomu, že ![]() , je také
, je také ![]() a je tedy možné velikost síly
a je tedy možné velikost síly ![]() zanedbat (viz obr. 58 c, d). Vrstva molekul, jejíž vzdálenost od volného povrchu kapaliny je menší než poloměr
zanedbat (viz obr. 58 c, d). Vrstva molekul, jejíž vzdálenost od volného povrchu kapaliny je menší než poloměr ![]() sféry molekulového působení, se nazývá povrchová vrstva kapalin. Na každou molekulu, která se nachází v povrchové vrstvě kapalin působí sousední molekuly přitažlivou silou, která míří dovnitř kapaliny.
sféry molekulového působení, se nazývá povrchová vrstva kapalin. Na každou molekulu, která se nachází v povrchové vrstvě kapalin působí sousední molekuly přitažlivou silou, která míří dovnitř kapaliny.
Při přemístění molekuly z vnitřku kapaliny do její povrchové vrstvy, je nutno vykonat práci k překonání právě popsané síly. Proto mají molekuly z povrchové vrstvy větší potenciální energii než molekuly v této vrstvě neležící. Povrchové vrstvě přiřazujeme tzv. povrchovou energii E, která je jednou složkou vnitřní energie kapaliny a která je dána vztahem ![]() (S je plocha volného povrchu kapaliny a
(S je plocha volného povrchu kapaliny a ![]() je povrchové napětí).
je povrchové napětí).
Kapalina daného objemu má snahu nabývat takového tvaru, aby obsah jejího povrchu byl co nejmenší, a tím byla minimální i povrchová energie. Při daném objemu má ze všech geometrických těles nejmenší obsah povrchu koule. Proto volné kapky mlhy, rosy, … mají kulový tvar. U větších kapek se projeví její tíhová síla a síla, kterou na ní působí podložka, a proto je kulový tvar deformován. (Dojde-li k vykompenzování těchto sil např. silou vztlakovou, zaujímají kulový tvar i větší kapky.)
Úlohy ze sbírky úloh KDF MFF
Multimedialní obsah
 kapky
kapky
|
[4 kB] | [Uložit] |  kapicky rtuti
kapicky rtuti
|
[149.02 kB] | [Uložit] |
 zvlastni tvary bublin
zvlastni tvary bublin
|
[4 kB] | [Uložit] | |||