Zaplňování orbitalů elektrony
Orbitaly, které se používají k popisu elektronové konfigurace prvků, mají své názvy. Tyto názvy orbitalů (s, p, d, f, …) souvisejí s vedlejším kvantovým číslem l, počet elektronů v jednotlivých orbitalech je pak dán dvojnásobkem počtu magnetických kvantových čísel m příslušných k danému vedlejšímu číslu l.
Dvojnásobek počtu magnetických kvantových čísel je zde proto, že musíme zohlednit i dvojí možný spin elektronu (![]() ).
).
Platí tedy:
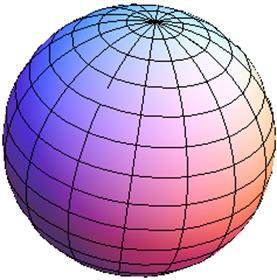
1. pro l = 0 máme celkem jedno magnetické číslo (m = 0), a proto orbital s má ![]() elektrony; orbital s má kulově symetrický tvar (tj. jedná se o kouli - viz obr. 52);
elektrony; orbital s má kulově symetrický tvar (tj. jedná se o kouli - viz obr. 52);
2. pro l = 1 máme celkem tři magnetická čísla (![]() ), a proto orbital p má
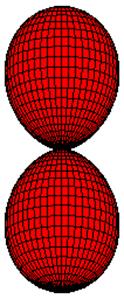
), a proto orbital p má ![]() elektronů; orbital p má tvar zobrazený na obr. 53 (natočení orbitalu je pak dáno konkrétním vedlejším kvantovým číslem m);
elektronů; orbital p má tvar zobrazený na obr. 53 (natočení orbitalu je pak dáno konkrétním vedlejším kvantovým číslem m);
3. pro l = 2 máme celkem pět magnetických čísel (![]() ), a proto orbital d má
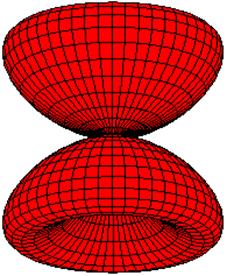
), a proto orbital d má ![]() elektronů; jedna z variant, jaký může mít orbital d tvar, je zobrazena na obr. 54;
elektronů; jedna z variant, jaký může mít orbital d tvar, je zobrazena na obr. 54;
4. pro l = 3 máme celkem sedm magnetických čísel (![]() ), a proto orbital f má
), a proto orbital f má ![]() elektronů;
elektronů;
5. pro l = 4 máme celkem devět magnetických čísel (![]() ), a proto orbital g má
), a proto orbital g má ![]() elektronů;
elektronů;
6. …
Počínaje orbitalem d jsou tvary orbitalů komplikované a přesný tvar velmi citlivě závisí na kombinaci všech kvantových čísel, kterými je daný orbital popsán. Pro další výklad nejsou tvary dalších orbitalů důležité.
 |  |  |
| Obr. 52 | Obr. 53 | Obr. 54 |
Každému hlavnímu kvantovému číslu n odpovídá ![]() různých stavů, ve kterých se elektrony mohou nacházet. To tedy znamená, že všechny stavy příslušející danému hlavnímu kvantovému n obsahují
různých stavů, ve kterých se elektrony mohou nacházet. To tedy znamená, že všechny stavy příslušející danému hlavnímu kvantovému n obsahují ![]() elektronů (viz tab. 1).
elektronů (viz tab. 1).
Pořadí jednotlivých orbitalů uvedených v tab. 1 neurčuje pořadí, v němž se tyto orbitaly zaplňují! Pořadí zaplňování jednotlivých orbitalů se řídí principem minima energie.
Tak, aby každá elektronová konfigurace byla v energeticky stabilní pozici.
Při zaplňování orbitalů elektrony platí určitá pravidla, kterými se zaplňování řídí. Některá z těchto pravidel platí pouze v kvantové fyzice (resp. atomové fyzice) a nemají svojí analogii v makrosvětě.
Tato „divná“ pravidla se tedy velmi obtížně populárně vysvětlují a velmi těžko si je představujeme, protože prostě s takovým chováním nemáme zkušenosti.
Tato pravidla jsou tři:
1. princip minima energie dané elektronové konfigurace;
2. Pauliho vylučovací princip;
3. Hundovo pravidlo.
Princip minima energie lze formulovat takto:
Dříve se zaplňují orbitaly s nižší energií, než orbitaly s vyšší energií. Energie orbitalu se přitom zvyšuje s rostoucím hlavním kvantovým číslem ![]() a vedlejším kvantovým číslem
a vedlejším kvantovým číslem ![]() . Je-li součet
. Je-li součet ![]() stejný pro dva různé orbitaly, zaplní se dříve orbital s menším hlavním kvantovým číslem
stejný pro dva různé orbitaly, zaplní se dříve orbital s menším hlavním kvantovým číslem ![]() .
.
Na základě tohoto principu a znalosti alternativního vyjádření vedlejšího kvantového čísla l pomocí názvu orbitalu je zřejmé, že pořadí zaplňování orbitalů je toto:
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p …
Např. orbital 4s se zaplní dříve než orbital 3d. Pro orbital 4s je ![]() a
a ![]() (orbital s) a pro orbital 3d je
(orbital s) a pro orbital 3d je ![]() a
a ![]() (orbital d). Tedy platí
(orbital d). Tedy platí ![]() , a proto se orbital 4s zaplní dříve než orbital 3d.
, a proto se orbital 4s zaplní dříve než orbital 3d.
Hundovo pravidlo, pojmenované po německém fyzikovi Friedrichu Hermannu Hundovi (1896 - 1997), se týká pomůcky, která se pro vizualizaci elektronové konfigurace používá. Jedná o zápis elektronové konfigurace do čtvercových polí tak, že se rozlišují dvě různé hodnoty spinu elektronu symbolizované dvěma opačně orientovanými šipkami: ![]() a
a ![]() . Tento zápis se přitom řídí právě Hundovým pravidlem:
. Tento zápis se přitom řídí právě Hundovým pravidlem:
V degenerovaných orbitalech vznikají elektronové páry až poté, co byl zaplněn každý orbital jedním elektronem. Všechny nespárované elektrony přitom mají stejný spin. V takovém případě má systém nejnižší energii, a proto je nejstabilnější.
Degenerované orbitaly jsou orbitaly, které jsou popsány stejným hlavním kvantovým číslem a stejným vedlejším kvantovým číslem. Navzájem se tedy liší pouze magnetickým kvantovým číslem.
Každý „čtvereček“ tak vlastně představuje jedno z kvantových čísel m; hlavní kvantové číslo je určeno „číslicí před čtverečkem“ a vedlejší kvantové číslo popisuje daný orbital (s, p, d, …). Každá ze zapisovaných „šipek“ představuje elektron, jehož kladný nebo záporný spin je vyjádřen různou orientací „šipky“.
Na obr. 55 je zobrazeno, jak správně zaplňovat jednotlivé orbitaly.
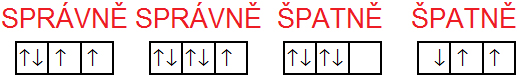 |
| Obr. 55 |
Příklady elektronových konfigurací některých prvků jsou zobrazeny na obr. 56. Ve všech případech se jedná o elektronové konfigurace elektricky neutrálních atomů.
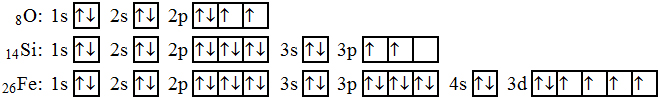 |
| Obr. 56 |
Pomocí Hundova pravidla lze zobrazit také elektronové konfigurace iontů - jak kladně nabitých iontů (kationty), tak záporně nabitých iontů (anionty). Přitom je nutné si uvědomit, jak ionty vznikají:
1. kationt vzniká tak, že z elektroneutrálního atomu je odtržen jeden nebo více elektronů; v atomovém obalu má tedy kationt příslušného prvku o daný počet elektronů méně, než má elektroneutrální atom;
V kationtu tedy převažuje náboj jádra nad nábojem elektronů v obalu, a proto je kationt nabit kladně.
2. aniont vzniká tak, že elektroneutrální atom přijme jeden nebo více elektronů; v atomovém obalu má tedy aniont příslušného prvku o daný počet elektronů více, než má elektroneutrální atom.
Náboj elektronů v obalu tedy v aniontu převažuje nad nábojem jádra, a proto má aniont záporný náboj.
Elektronové konfigurace jednoho kationtu a jednoho aniontu jsou zobrazeny na obr. 57. Porovnáním s elektronovou konfigurací zobrazenou na obr. 56 si můžeme uvědomit příslušné rozdíly.
U železitého kationtu (stejně jako u kationtů všech přechodných prvků) se přesouvají všechny zbylé elektrony do orbitalu d.
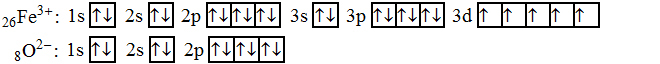 |
| Obr. 57 |
Pomocí elektronové konfigurace lze také zapisovat atomy v excitovaném stavu. V tomto stavu mají elektrony vyšší energii, než ve stavu základním; nacházejí se tedy dále od jádra atomu. Tomu odpovídá i zápis elektronové konfigurace (viz obr. 58, na kterém je zobrazen uhlík v základním stavu a v excitovaném stavu; v základním stavu je uhlík dvojvazný a v excitovaném stavu je uhlík čtyřvazný).
Excitovaný stav je stav s vyšší energií - elektrony získají energii od okolí (ohřev, „posvícení“ elektromagnetickým zářením, …) a přesunou s dále od jádra atomu. Celý atom tak bude snáze (případně jinak) reagovat, než kdyby byl ve svém základním stavu.
V elektronové konfiguraci vytvoříme excitovaný stav tak, že „rozbijeme“ poslední dvojici „šipek“ a jednu z těchto „šipek“ přesuneme do nejbližšího volného čtverečku (ve shodě s Hundovým pravidlem).
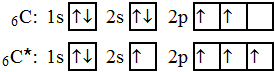 |
| Obr. 58 |
Na obr. 59 jsou zobrazeny elektronové konfigurace vzácných plynů: ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() . To jsou plyny, jejichž valenční slupka je zcela zaplněna a tyto prvky jsou chemicky netečné (tj. za běžných podmínek chemicky s ostatními prvky nereagují). Z obr. 59 je patrné, že poslední orbital, který zaujímají elektrony v elektronové konfiguraci vzácných plynů, je vždy orbital p (s výjimkou He, jehož elektronová konfigurace končí orbitalem 1s).
. To jsou plyny, jejichž valenční slupka je zcela zaplněna a tyto prvky jsou chemicky netečné (tj. za běžných podmínek chemicky s ostatními prvky nereagují). Z obr. 59 je patrné, že poslední orbital, který zaujímají elektrony v elektronové konfiguraci vzácných plynů, je vždy orbital p (s výjimkou He, jehož elektronová konfigurace končí orbitalem 1s).
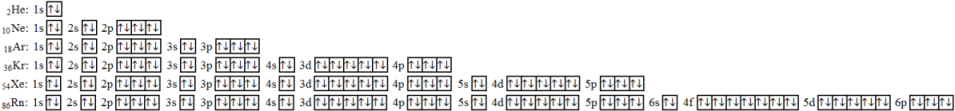 |
| Obr. 59 |
Skutečnosti, že vzácné plyny mají zcela zaplněné valenční slupky, se využívá ke zjednodušenému zápisu elektronové konfigurace ostatních prvků. Využijeme známou konfiguraci vzácného plynu, který má nejbližší menší protonové číslo, než daný prvek. Do elektronové konfigurace daného prvku pak zapíšeme pouze ty elektrony, které jsou navíc oproti konfiguraci nalezeného vzácného prvku. Příklady elektronových konfigurací několika prvků zapsaných pomocí vzácných plynů jsou zobrazeny na obr. 60.
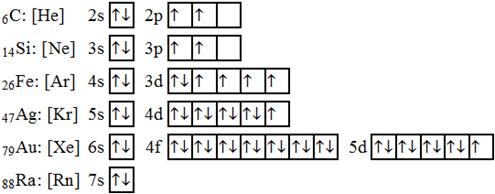 |
| Obr. 60 |