Spektrum atomu vodíku
Poznatek o tom, že energie atomů je kvantována a že může nabývat jen určitých dovolených hodnot (energetických hladin), byl získán mnohem dříve, než vznikla kvantová mechanika, a byl potvrzen řadou experimentů. První z těchto experimentů se týkaly spektra záření vydávaného atomy v elektrických výbojích a v plynech.
Realizace elektrických výbojů v různých plynech v laboratoři byla možná už ve druhé polovině 19. století. Blesk v přírodě byl znám odpradávna, byť se dlouho spekulovalo o jeho příčině vzniku.
Spektrum záření různých látek se dělí podle dvou kritérií (viz obr. 37).
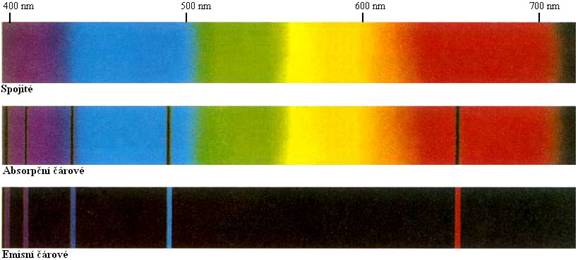 |
| Obr. 37 |
Prvním kritériem dělení je způsob vzniku spektra; rozeznáváme spektrum:
1. emisní - spektrum, které je vyzařováno (emitováno) daným tělesem;
2. absorpční - spektrum vznikající tak, že určité těleso část elektromagnetického záření (o určitých vlnových délkách) pohltí (absorbuje) a dál proniká elektromagnetické záření, v němž tyto pohlcené složky chybí.
Podle tvaru spektra rozeznáváme spektrum:
1. spojité - je tvořeno elektromagnetickým zářením všech vlnových délek (resp. všech vlnových délek z určitého intervalu);
Zdrojem spojitého elektromagnetického spektra je např. Slunce, žárovky, …
2. čárové - spektrum je tvořeno pouze zářením o určitých vlnových délkách
Čárové spektrum mají plyny nebo zahřáté páry kovů, v nichž probíhá elektrický výboj (sodíková výbojka, neonka, …).
Čárové spektrum je tvořeno čárami, které ve spektru buď chybějí a nebo jsou v něm zastoupeny osamoceně. Chybějí-li ve spektru určité čáry, jedná se o absorpční spektrum - některé čáry byly absorbovány materiálem, kterým záření procházelo na cestě od zdroje k pozorovateli. Obsahuje-li spektrum pouze izolované čáry, jedná se o spektrum emisní - daný zdroj vysílá pouze záření o určitých vlnových délkách.
Soustava spektrálních čar je pro každý druh atomů, každý prvek charakteristická. Na základě znalosti spektra lze každý prvek přesně identifikovat a provádět tak chemickou spektrální analýzu. Tímto způsobem bylo objeveno helium dříve na Slunci než na Zemi.
Každý prvek má tak vlastně jakýsi „otisk“ jako má prst u člověka. Proto lze pomocí absorpčních spekter zkoumat chemické složení různých těles vyzařujících nebo pohlcujících elektromagnetické záření - např. i vesmírných těles: Slunce, hvězd, …
Koncem padesátých let 19. století vynalezli němečtí fyzikové Gustav Robert Kirchhoff (1824 - 1887) a Robert Bunsen (1811 - 1899) spektroskop a s využitím metod spektrální analýzy objevili v roce 1860 nový prvek s šedomodrou spektrální čárou, který nazvali cesium. O rok později objevil na základě spektrální analýzy nový prvek i britský fyzik a chemik William Crookes (1832 - 1919). Jeho spektrum bylo tvořeno jasně zelenou čarou, a proto dostal prvek název thallium (řecky thallos znamená zelená ratolest).
Jako jedno z prvních bylo zkoumáno spektrum nejlehčího z prvků - vodíku. Švýcarský matematik a fyzik Johann Balmer (1825 - 1898) si v roce 1885 všiml, že pro frekvence spektrálních čar vodíku platí jednoduchá zákonitost: ![]() , kde
, kde ![]() a
a ![]() je Rydbergova frekvence. Frekvence (resp. vlnové délky) elektromagnetického záření vypočtené na základě uvedeného vztahu velmi dobře odpovídají hodnotám naměřeným při experimentech.
je Rydbergova frekvence. Frekvence (resp. vlnové délky) elektromagnetického záření vypočtené na základě uvedeného vztahu velmi dobře odpovídají hodnotám naměřeným při experimentech.
Začátkem 20. století byly zjištěny další čáry vodíkového spektra a to v ultrafialové a infračervené oblasti spektra elektromagnetického záření. Také tyto čáry se řadily do sérií a jejich frekvence bylo možné vyjádřit obecnějším vztahem ![]() , kde
, kde ![]() ,
, ![]() . Jednotlivé série byly nazvány podle svých objevitelů (viz obr. 38):
. Jednotlivé série byly nazvány podle svých objevitelů (viz obr. 38):
1. ![]() - série Lymanova (ultrafialová část spektra)
- série Lymanova (ultrafialová část spektra)
2. ![]() - série Balmerova (viditelná část spektra)
- série Balmerova (viditelná část spektra)
3. ![]() - série Paschenova (infračervená část spektra)
- série Paschenova (infračervená část spektra)
4. ![]() - série Brackettova (infračervená část spektra)
- série Brackettova (infračervená část spektra)
5. ![]() - série Pfundova (infračervená část spektra)
- série Pfundova (infračervená část spektra)
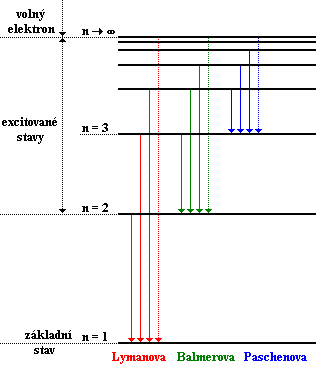 |
| Obr. 38 |
Uvedené zákonitosti je možné vysvětlit, pokud budeme předpokládat, že atom vodíku se může nacházet na určitých energetických hladinách ![]() a při přechodech (skocích) z vyšší energetické hladiny na nižší vyzařuje elektromagnetické záření podle vztahu
a při přechodech (skocích) z vyšší energetické hladiny na nižší vyzařuje elektromagnetické záření podle vztahu ![]() , tj. po dosazení
, tj. po dosazení ![]() . Pro energetické hladiny vodíku odtud dostáváme:
. Pro energetické hladiny vodíku odtud dostáváme: ![]() .
.
Tyto hladiny jsou záporné, takže vyššímu n odpovídá vyšší hodnota energie a pro ![]() je
je ![]() (viz obr. 38). V takovém případě je již vazba elektronu v atomu natolik slabá, že dochází k ionizaci, tj. vytržení elektronu z atomu vodíku. Elektron se stává volným a jeho energie přestává být kvantována. Elektron v tak může získat už libovolnou kladnou kinetickou energii
(viz obr. 38). V takovém případě je již vazba elektronu v atomu natolik slabá, že dochází k ionizaci, tj. vytržení elektronu z atomu vodíku. Elektron se stává volným a jeho energie přestává být kvantována. Elektron v tak může získat už libovolnou kladnou kinetickou energii ![]() .
.
S rostoucím n se zmenšuje zlomek ![]() , ale zlomek
, ale zlomek ![]() se zvětšuje. Je to záporné číslo, které zmenšuje svojí absolutní hodnotu - blíží se nule.
se zvětšuje. Je to záporné číslo, které zmenšuje svojí absolutní hodnotu - blíží se nule.
Základní stav atomu vodíku pro ![]() odpovídá energii
odpovídá energii ![]() , což je záporně vzatá ionizační energie vodíku. Abychom „rozbili“ (ionizovali) atom vodíku, musíme mu skutečně dodat energii
, což je záporně vzatá ionizační energie vodíku. Abychom „rozbili“ (ionizovali) atom vodíku, musíme mu skutečně dodat energii ![]() .
.
Multimedialní obsah
 spektra zdroju svetla
spektra zdroju svetla
|
[4 kB] | [Uložit] |  spektrum slunce
spektrum slunce
|
[4 kB] | [Uložit] |
 spektrum atomu vodiku
spektrum atomu vodiku
|
[114.34 kB] | [Uložit] | |||