Spin
Experimenty s chováním atomů v magnetickém poli ukázaly, že kvantových stavů elektronu je ve skutečnosti dvojnásobný počet. Je to proto, že elektron představuje vlastně jakýsi malý magnet, který se ve vnějším magnetickém poli může orientovat dvojím způsobem - ve směru pole a proti jeho směru. Tato vlastnost elektronu se označuje jako spin (anglicky spin = točit, vířit, kroužit).
Elektron připomíná rotaci nabitého vlčku v jednom nebo druhém směru. Jedná se ovšem pouze o naši představu, neboť u objektů mikrosvěta není možné hovořit o jejich rotaci. Jedná o určitý kvantový pohyb, pro nějž nemáme v makrosvětě analogii.
Přesné zavedení spinu částice lez udělat pouze s přesnými matematickými výpočty a formulacemi, které vycházejí z kvantové mechaniky.
Dvě opačné orientace elektronu v magnetickém poli se budou lišit i energií, a proto je lze popsat čtvrtým kvantovým číslem - tzv. spinovým magnetickým kvantovým číslem ![]() , které nabývá pouze dvou hodnot:
, které nabývá pouze dvou hodnot: ![]() . Kvantový stacionární stav atomu vodíku je tedy popsán čtyřmi kvantovými čísly n, l, m,
. Kvantový stacionární stav atomu vodíku je tedy popsán čtyřmi kvantovými čísly n, l, m, ![]() , přičemž pro každému n odpovídá celkem
, přičemž pro každému n odpovídá celkem ![]() různých stavů, ve kterých se elektron může nacházet.
různých stavů, ve kterých se elektron může nacházet.
Ve velmi hrubém přiblížení lze říci, že spin poskytuje informaci o tom, jak vypadá částice z různých směrů:
1. ![]() - částice vypadá jako tečka, tj. ze všech směrů se jeví stejná (viz obr. 46a)
- částice vypadá jako tečka, tj. ze všech směrů se jeví stejná (viz obr. 46a)
2. ![]() - částici lze znázornit jako šipku, tj. při otáčení se jeví různě (viz obr. 46b). Abychom znovu dosáhli původního vzhledu, je třeba ji otočit o plných
- částici lze znázornit jako šipku, tj. při otáčení se jeví různě (viz obr. 46b). Abychom znovu dosáhli původního vzhledu, je třeba ji otočit o plných ![]() .
.
3. ![]() - částice se podobá obousměrné šipce (viz obr. 46c), tj. ztotožnění s původním obrazem nastane již po otočení o
- částice se podobá obousměrné šipce (viz obr. 46c), tj. ztotožnění s původním obrazem nastane již po otočení o ![]()
4. ![]() - ztotožnění částice nastane již po otočení o
- ztotožnění částice nastane již po otočení o ![]() (viz obr. 46d)
(viz obr. 46d)
5. …
6. ![]() - částice bude vyhlížet stejně ne po jednom otočení o plný úhel, ale až po dvou otočení o plný úhel. Zde již selhává představa klasické geometrie a fyziky.
- částice bude vyhlížet stejně ne po jednom otočení o plný úhel, ale až po dvou otočení o plný úhel. Zde již selhává představa klasické geometrie a fyziky.
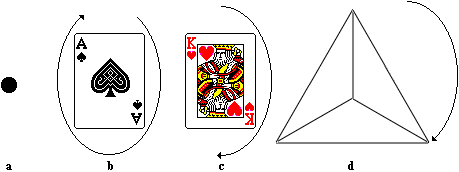 |
| Obr. 46 |
Na základě spinu (resp. spinového magnetického kvantového čísla) ![]() lze částice rozdělit do dvou skupin - na fermiony a bosony.
lze částice rozdělit do dvou skupin - na fermiony a bosony.