Olověný akumulátor
Akumulátor s olověnými elektrodami poprvé sestrojil francouzský fyzik Gaston Planté (1834 - 1889) v roce 1859. Po dalších úpravách se tento akumulátor začal hojně používat v praxi.
Jedná se vlastně o galvanický článek se dvěma olověnými elektrodami, které jsou ponořené v roztoku zředěné kyseliny sírové. Ta může být v akumulátoru ve formě roztoku nasáknutého do skelného vlákna, kterým jsou olověné desky proloženy, nebo je ztužena do formy gelu. Elektrody jsou vyrobeny z olověné slitiny ve tvaru mřížky, aby měly co největší povrch a mohly na nich intenzivně probíhat chemické reakce. Slitina se používá proto, že samotné olovo je příliš měkké a nedrželo by příslušný tvar; proto se přidávají další prvky (antimon, vápník, cín, selen, …), aby výsledný materiál měl vyšší mechanickou pevnost a lepší elektrickou vodivost.
Jedna elektroda je tvořena olověnou deskou, druhá deska je pokryta vrstvou oxidu olovičitého ![]() .
.
Schéma akumulátoru, který může mít elektromotorické napětí 6 V, 12 V nebo 24 V, je zobrazeno na obr. 109.
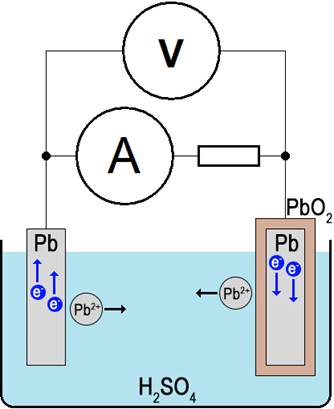 |
| Obr. 109 |
Při vybíjení se materiál elektrod (olovo i oxid olovičitý) přeměňuje na síran olovnatý. Elektrolyt je přitom ochuzován o kyselinu sírovou a obohacován o vodu.
Elektrolyt akumulátoru se disociuje: ![]() .
.
Na olověné elektrodě probíhá při vybíjení akumulátoru oxidace olova: ![]() . Tato elektroda se tedy nabíjí záporně. Následně na této elektrodě vzniká vrstva síranu olovnatého:
. Tato elektroda se tedy nabíjí záporně. Následně na této elektrodě vzniká vrstva síranu olovnatého: ![]() .
.
Na elektrodě pokryté oxidem olovičitým nastává redukce olovičitých kationtů: ![]() a proto se deska nabíjí kladně. Následně se i tato elektroda pokrývá vrstvou síranu olovnatého:
a proto se deska nabíjí kladně. Následně se i tato elektroda pokrývá vrstvou síranu olovnatého: ![]() .
.
Obě popsané reakce lze zapsat do jedné: ![]() .
.
Jakmile vrstva síranu olovnatého na obou elektrodách zabrání průchodu elektrického proudu, je akumulátor vybit.
Při následném nabíjení akumulátoru pomocí externího zdroje elektrického napětí se zvyšuje koncentrace kyseliny sírové tvořící elektrolyt rozpouštěním síranu olovnatého z elektrod a rozkladem molekul vody za vzniku kyseliny sírové. Souhrnně lze reakce probíhající při nabíjení akumulátoru popsat rovnicí: ![]() .
.
Jedná se tedy o reakci probíhající opačně, než probíhá reakce při vybíjení akumulátoru.
Tím, že se koncentrace kyseliny sírové v akumulátoru při jeho činnosti mění, lze pomocí této koncentrace měřit stav nabití akumulátoru.
Během dobíjení akumulátoru může probíhat i elektrolýza vody, zejména po rozpuštění všeho síranu olovnatého z elektrod. Na kladné elektrodě se pak tedy vylučuje plynný kyslík, na záporné elektrodě se pak vylučuje plynný vodík. Oba plyny z akumulátoru unikají, a proto se snižuje množství vody v akumulátoru. Proto je nutné kontrolovat stav elektrolytu a v případě potřeby dolívat destilovanou vodu.